Światowa transplantologia jest w kryzysie, którego nie sposób opanować. Brakuje organów do przeszczepów, a liczba potrzebujących stale rośnie. Naukowcy z całego świata starają się znaleźć alternatywę dla klasycznych przeszczepów, np. poprzez hodowlę organów w ciałach zwierząt (ksenotransplantacje) lub wykorzystanie komórek macierzystych do rozwinięcia się w funkcjonalne narządy. To wciąż jednak melodia przyszłości, a nadal podstawowym źródłem narządów do przeszczepów pozostają dawcy, u których stwierdzono śmierć pnia mózgu.
Problemem w przypadku narządów do przeszczepów jest ich przechowywanie. Mają one bowiem ograniczony czas “przydatności” od momentu pobrania (różny w zależności od rodzaju narządu). Teraz powstał pomysł, jak to zmienić.
Jak wydłużyć przydatność organu do przeszczepu?
Jednym z głównych wyzwań związanych z przechowywaniem tkanek i organów do przeszczepów jest zapobieganie gromadzeniu się kryształów lodu, które mogą powodować poważne uszkodzenia. Teraz naukowcy z Uniwersytetu Kalifornijskiego opracowali obiecującą technikę superchłodzenia, aby przywrócić funkcjonalność zmodyfikowanej tkance serca. To może być przełom, pozwalający na dłuższe przechowywanie organów do przeszczepów.
Technologia, o której mowa, to tzw. zamrażanie izochoryczne, stworzona przez Borisa Rubinsky’ego z Uniwersytetu Kalifornijskiego w Berkeley ok. 16 lat temu. Czym się wyróżnia?
W przypadku konwencjonalnego zamrażania izobarycznego, materiał jest wystawiany na działanie zimnego powietrza pod stałym ciśnieniem. W przypadku zamrażania izochorycznego, materiał jest zanurzany w cieczy, a następnie zamykany w pozbawionym powietrza pojemniku, w którym nie ma szans na powstawanie kryształów lodu, nawet jeżeli temperatura spadnie poniżej zera. We wcześniejszych eksperymentach aż 40% materiału pozostało niezamrożonego, mimo że schłodzono go do temperatury -22oC.
To jest fundamentalna termodynamika. Kiedy materiał, który ma zostać zamrożony, jest zamknięty w szczelnym pudełku, wtedy zamarza tylko część objętości.Boris Rubinsky
Przełomowe zamrażanie
Teraz naukowcy poszli krok dalej i wykorzystali system “narządu na chipie” (ang. organ-on-a-chip), czyli specjalny pojemnik do hodowli komórkowej 3D, który symuluje czynności, mechanikę i reakcję fizjologiczną całych narządów. Tego typu struktury nie są substytutami funkcjonalnych narządów, ale modelami, na których można testować działanie nowych leków, itd.
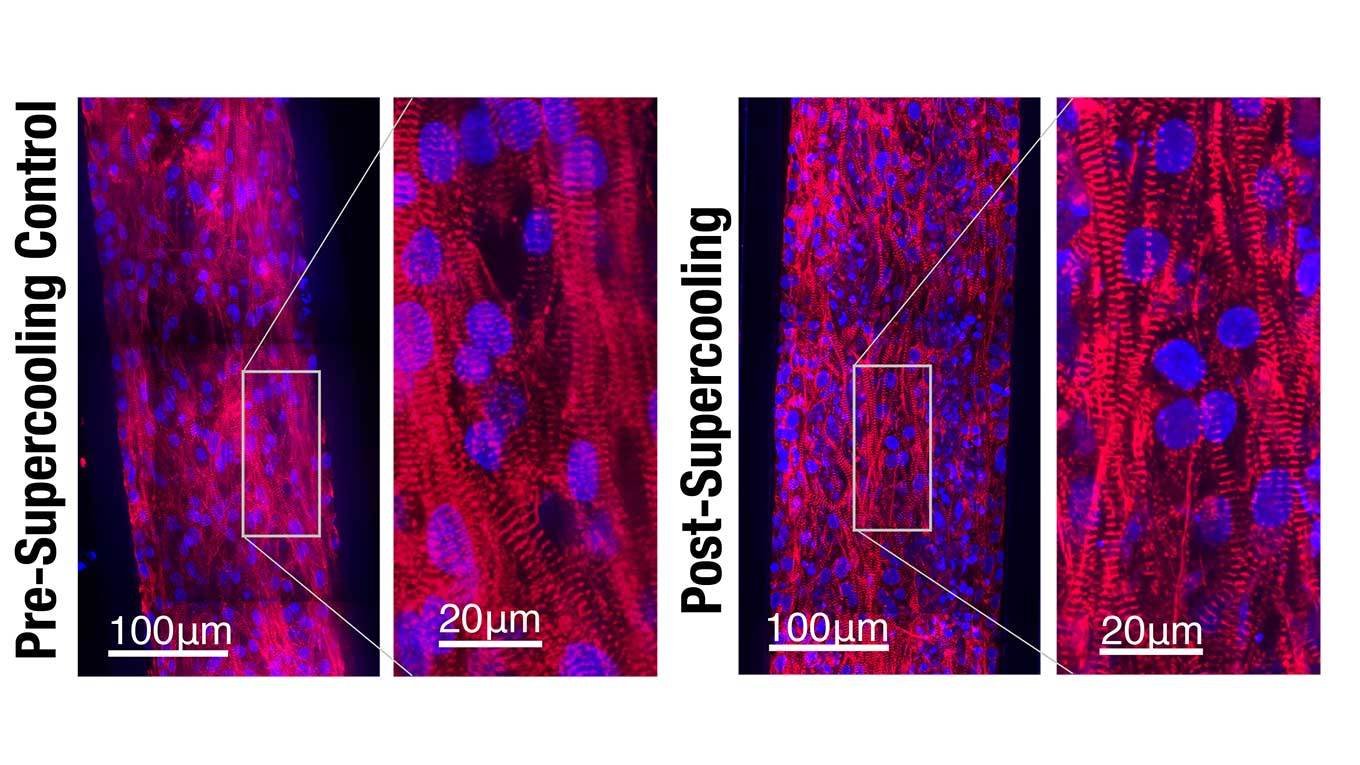
Naukowcy użyli model serca, wytworzony z indukowanych pluripotencjalnych komórek macierzystych, czyli takich, które wywodzą się z dorosłych komórek, ale zostały cofnięte do stanu komórek macierzystych. Tak stworzony organoid wykazywał funkcjonalność miniaturowego serca. Poddano go zamrożeniu izochorycznemu i całość schłodzono do temperatury -3oC. Komórki serca pobrano po 24, 48 i 72 godzinach i umieszczono ponownie w temperaturze ok. 37oC.
Okazało się, że funkcjonalność zachowało 65-80% próbek, bez większej różnicy między tymi, które były zamrożone dłużej, a które krócej. Kluczowy był sam sposób zamrażania izochorycznego, który nie wpłynął na strukturalną integralność tkanki serca. Tkanka pozostała również wrażliwa na leki stosowane w celu zwiększenia częstości akcji serca.
Technika zastosowana przez naukowców z Uniwersytetu Kalifornijskiego wskazuje na słuszność stosowania zamrażania izochorycznego do przechowywania narządów do przeszczepów. Więcej można przeczytać w dzienniku Communications Biology.
