Energetyka z OZE ma jedną cechę, o której musimy pamiętać – to niezależna od nas pogoda odgrywa kluczową rolę, nadając rytm całemu cyklowi produkcji. Słońce daje moc wtedy, kiedy świeci, a wiatr wtedy, kiedy wieje, ale odbiorców prądu w ogóle to nie obchodzi. Dostęp do energii elektrycznej ma być ciągły i przewidywalny, bo nie tylko piece, instalacje chemiczne czy linie produkcyjne są od niego zależne, ale każdy z nas. Właśnie w tej luce (między niestabilnym źródłem a stabilnym zużyciem) rodzą się najciekawsze pomysły, które czasem są zupełnie nieintuicyjne.
Słońce już zaszło, a oni i tak zrobili wodór. Ten trik z chemią może namieszać
Coraz częściej wraca pytanie nie o to, jak wytworzyć wodór, tylko jak go “rozłożyć w czasie”. W skrócie chodzi o to, aby zmagazynować pozyskaną energię wtedy, gdy jest tania i dostępna, a oddać ją wtedy, gdy jest potrzebna. Wszystko to najlepiej bez rozbudowanej infrastruktury, bez kilometrowych instalacji i z pełną kontrolą nad procesem. Najnowsza praca zespołów niemieckich specjalistów dokłada do tej dyskusji coś świeżego, bo wyjątkowy laboratoryjny układ, który rozdziela moment ładowania światłem od momentu produkcji wodoru.
Czytaj też: Niesamowite osiągnięcie w fotowoltaice. Słońce niszczyło, ale teraz zaczęło chronić
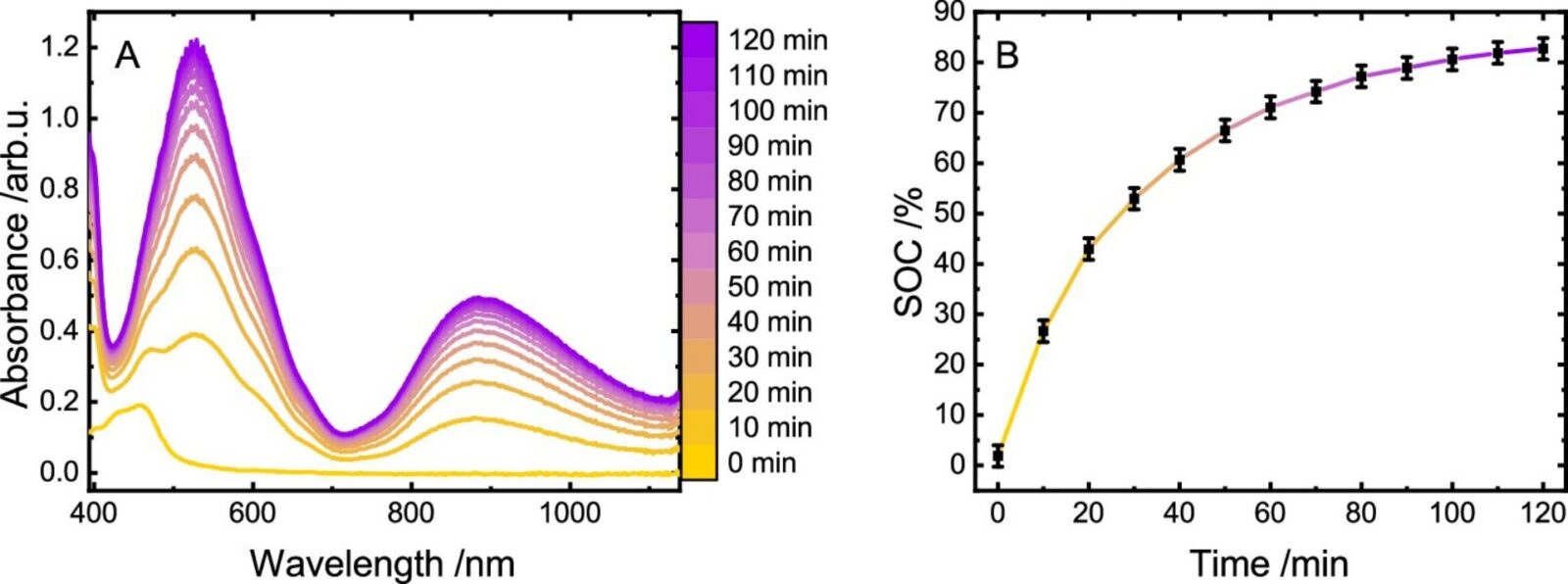
W centrum pomysłu stoi wodnorozpuszczalny, redoksowo aktywny kopolimer, czyli długi łańcuch złożony z dwóch typów “klocków” chemicznych, z których jeden odpowiada za rozpuszczalność w wodzie, a drugi pełni rolę magazynu elektronów. W praktyce jest to miękki, polimerowy odpowiednik materiału, którego znamy z idei akumulatorów przepływowych, co oznacza tyle, że nie trzymamy energii w zwartej elektrodzie, tylko w roztworze, który można “naładować” i później “rozładować”. W specyficznej konfiguracji naukowcy uzyskali sprawność ładowania powyżej 80% i zdołali utrzymać stan naładowania przez co najmniej 3 dni.

Gdy roztwór zostanie zakwaszony (w eksperymentach do pH na poziomie około 2) i dostanie katalizator wydzielania wodoru, zgromadzone elektrony “spotykają się” z protonami, a efektem jest właśnie wodór. Cały proces jest uruchamiany wtedy, kiedy ktoś tego chce, a nie wtedy, kiedy system osiągnie specyficzny poziom. Najlepszy wynik w tej pracy dał katalizator platynowy w formie nanocząstek, który odznaczył się maksymalną sprawnością konwersji elektronów na wodór do ok. 72%. Autorzy wyliczają, że układ przechowuje ładunek około 28 mAh/g, czyli w przybliżeniu kilkanaście mililitrów wodoru na gram samego polimeru.
Czytaj też: Rozwiązali największy problem fotowoltaiki! Prąd popłynie nawet w deszczu
Cały system da się też zresetować i użyć ponownie prostym przełączeniem pH. Po rozładowaniu roztwór neutralizuje się, by znów mógł być ładowany światłem, bo w środowisku kwaśnym donor elektronów (TEA) przestaje działać w tej roli. W materiałach towarzyszących pracy pojawia się również efekt “wizualny”, bo zmiana barwy roztworu przy przejściu między stanami, co przypomina, że jest to układ chemiczny, którym steruje się warunkami środowiska, a nie tylko przełącznikiem w elektronice.
Nie wszystko złoto, co się świeci
Chociaż tego typu podejście z pozoru brzmi świetnie, to nie brakuje w nim problemów. Pierwszy jest fundamentalny – w tej wersji nie jest to pełne rozszczepianie wody “światło + woda = wodór”. Elektrony pochodzą z donora ofiarnego, który zużywa się w procesie ładowania. Jest to typowe w fotochemii na etapie badań koncepcyjnych, ale dopiero podmiana tego elementu na realne źródło elektronów (najczęściej: utlenianie wody z osobnym katalizatorem) przesuwa układ w stronę stricte użytecznej technologii.
Drugi haczyk to materiały. Ruten jako fotouczulacz i platyna jako najlepszy katalizator wodoru są świetne w laboratorium, ale nie są wymarzonym duetem do uzyskiwania taniego sprzętu. Do tego dochodzi chemia wiologenów, która wprawdzie jest sprawdzona jako nośnik elektronów (również w akumulatorach przepływowych), ale wymaga ostrożnego doboru warunków, stabilizacji i ochrony przed niepożądanymi reakcjami ubocznymi. Zresztą sami autorzy podkreślają rolę bufora i ograniczeń pH, bo polimer może ulegać nieodwracalnym przemianom przy zbyt wysokim pH.
Trzeci problem to “koszt obsługi” przełącznika pH. W eksperymencie zachodzi cykl z roztworu kwasowego do neutralnego, co w realnym układzie oznaczałoby gospodarkę kwasem i zasadą, rosnące zasolenie oraz konieczność kontroli składu roztworu. W samej publikacji widać też spadek parametrów w kolejnych cyklach, a autorzy wiążą część strat m.in. ze wzrostem siły jonowej. To nie przekreśla koncepcji, ale sugeruje, że “proste przełączanie pH” w skali przemysłowej szybko przestaje być proste.
Czytaj też: Chiny budują “super akumulator”. Największy taki obiekt na świecie powstanie w górach
Mimo tych wszystkich zastrzeżeń, praca pokazuje świetny most między światem fotokatalizy a światem magazynowania energii. Most zbudowany z polimeru, który już wcześniej pojawiał się w kontekście chemicznych magazynów ładunku.
Źródła: Nature, TechXplore

