Wystarczy raz zobaczyć kroplę wody, która zamiast syczeć i znikać, zaczyna tańczyć po bardzo rozgrzanej powierzchni. Ten widok jest nieintuicyjny, ale znacznie bardziej zaskakujące jest to, że można wykorzystać stojące za tym mechanizmy do produkcji akumulatorów, a dokładniej mówiąc, proszków elektrodowych.
Efekt Leidenfrosta jako narzędzie, nie sztuczka
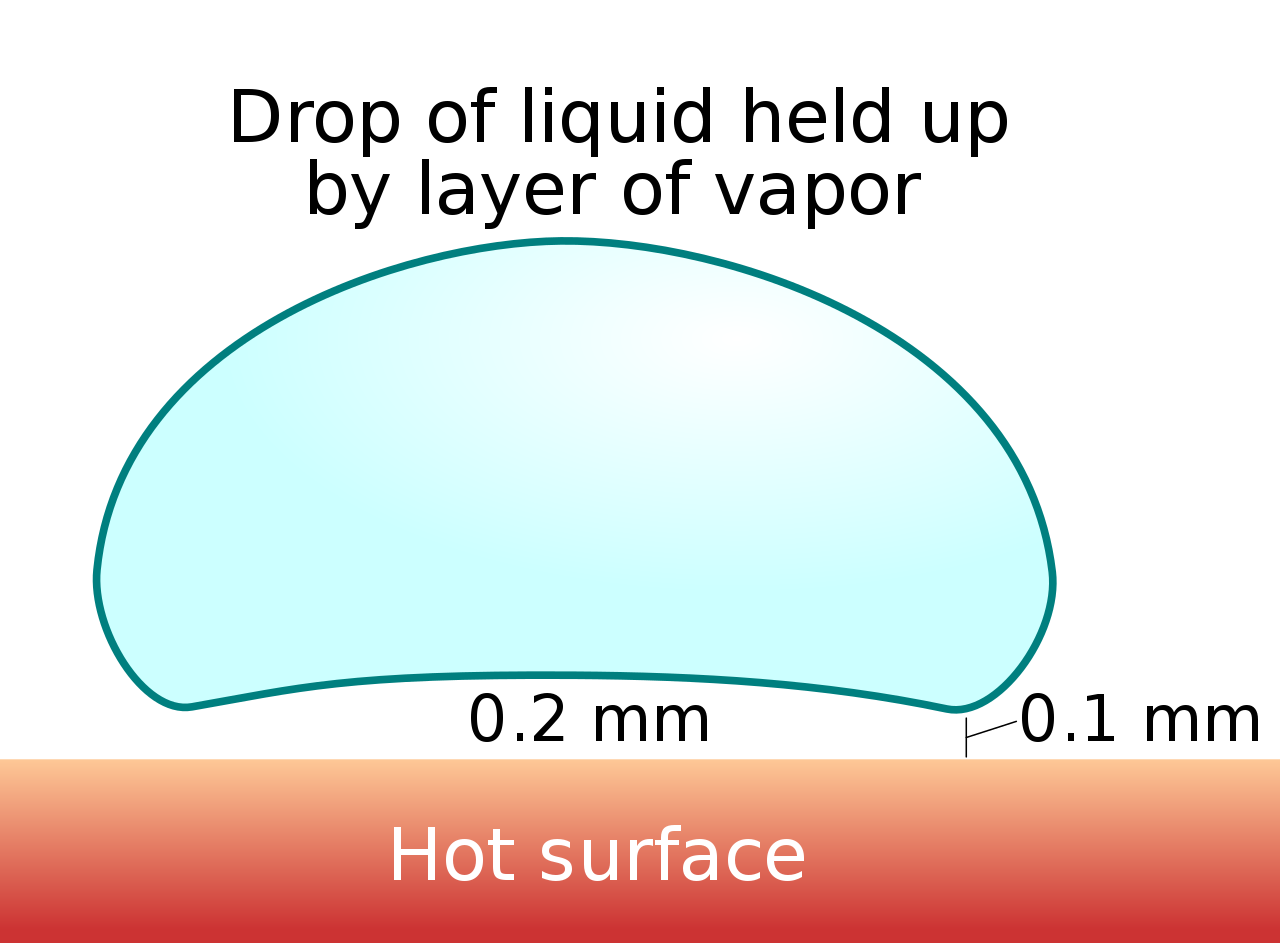
Efekt Leidenfrosta został opisany w 1756 roku, a w skrócie chodzi o to, że kropla cieczy na powierzchni znacznie gorętszej niż temperatura wrzenia unosi się na cienkiej poduszce własnej pary i przez to ma ograniczony kontakt z podłożem. To właśnie ten parowy “łożyskowy” stan sprawia, że kropla potrafi sunąć po metalu, zamiast natychmiast się zagotować i w grę nie wchodzą żadne ekstremalne temperatury. To zjawisko możecie zaobserwować sami w kuchni, np. korzystając we właściwy sposób ze stalowych patelni.
Czytaj też: Słońce dziś, a wodór za kilka dni. Niemcy zaskoczyli świat swoim wynalazkiem
Tym razem specjaliści postanowili potraktować to zjawisko jako element procesu syntezy materiału katodowego do akumulatorów sodowo-jonowych. Mowa dokładnie o wytwarzaniu proszku poprzez kontakt rozpylonego roztworu prekursorów z bardzo gorącą powierzchnią, gdzie krople szybko tracą rozpuszczalnik i formują cząstki o strukturze sprzyjającej późniejszej pracy elektrochemicznej. Innymi słowy, zapewnia to kolejny element układanki w trwającej walce o rozpowszechnienie nowego rodzaju akumulatorów, które zamiast na drogim i ograniczonym licie, bazują na tanim i powszechnym sodzie. Aktualnie jednak ich problem sprowadza się do niskiej gęstości energii rzędu (aktualnie) około 175 Wh/kg.
Katoda, czyli miejsce, w którym akumulator często przegrywa z czasem
W sodowo-jonowych akumulatorach problemem bywa katoda, bo większy jon sodu trudniej “przepchnąć” przez ciasne ścieżki migracji w strukturze krystalicznej. Dlatego badacze chętnie sięgają po materiały polianionowe, gdzie mocne wiązania (np. w grupach fosforanowych) pomagają utrzymać stabilność struktury, a sama architektura kryształu potrafi tworzyć tuneliki dla jonów. Jednym z kandydatów jest NFPP, który odznacza się zaletami w postaci stabilności i potencjalnie niskich kosztów, ale też z klasycznym problemem niskiej przewodności elektronowej i barier dla szybkiego transportu jonów.

W omawianej pracy rdzeń pomysłu jest z kolei dwutorowy, bo po pierwsze, autorzy modyfikują materiał w skali atomowej, zastępując niewielką część żelaza indem, a po drugie, proponują sposób syntezy, który ma ułatwiać uzyskanie korzystnej mikrostruktury proszku bez długich, energochłonnych etapów. Efekt? Pojemność właściwa na poziomie 129,3 mAh/g oraz gęstość energii rzędu 359 Wh/kg. Kluczowe jest to, że mówimy o gęstości energii przeliczonej dla materiału katody w warunkach laboratoryjnych, a nie o gotowym pakiecie czy nawet pełnym ogniwie użytkowym. W realnym produkcie do gry wchodzą jeszcze masa anody, elektrolitu, kolektorów prądowych, obudowy i marginesy bezpieczeństwa, więc wartości “na kilogram materiału aktywnego” są z natury wyższe niż to, co dostaje finalnie samochód.
Czytaj też: Rozwiązali największy problem fotowoltaiki! Prąd popłynie nawet w deszczu
Równie ważna jest informacja o trwałości: stabilne działanie przez ponad 10000 cykli przy 20C, bo mówi to, że test odbywał się przy bardzo dużych prądach (w uproszczeniu: szybkie ładowanie i rozładowanie), co jest ciekawą próbą wytrzymałości kinetycznej. Jednak kwestia produkcji tego typu nadal pozostaje pod znakiem zapytania. W klasycznych podejściach materiały elektrodowe potrafią wymagać długiego wygrzewania w piecach i precyzyjnej kontroli atmosfery, a to kosztuje energię i czas. W proponowanym podejściu z wykorzystaniem efektu Leidenfrosta klucz ma tkwić w szybkim formowaniu cząstek proszku z kropli na gorącej powierzchni, co sprzyja powstawaniu porowatej struktury ułatwiającej zwilżanie elektrolitem i transport jonów. Nadal wymaga to energii oraz kontroli, ale to już sprawa na inne badanie.
Źródła: EurekAlert!, RSC Publishing

